近年研究发现AS受鞘磷脂(sphingomyelin,SM)水平的直接影响。鞘磷脂及鞘磷脂的代谢酶在AS进程中扮演了重要的角色,包括引起脂蛋白成分的改变,和其介导的一系列细胞过程。流行病学调查也显示,体内SM 水平与AS存在呈独立的相关性,血浆SM 水平在评价AS发展过程中具有指标意义。抑制SM的合成就能产生抗AS效果。鞘磷脂合酶(sphingomyelin synthase,SMS)是体内从头合成SM 的最后步骤的关键酶,它直接调控SM水平的高低,这是AS病变发生的关键指标之一。由于SMS 催化的反应处于磷脂生物合成循环的最后环节,抑制其生物活性引起的潜在毒副反应可能较小。对小鼠SMS2的两个等位基因全敲除后仍正常存活,说明SMS2是有效的和安全的药物靶点,通过抑制SMS2活性降低SM水平有可能成为治疗动脉粥样硬化的新方法。此外,现有研究表明,SMS2的抑制还与抗糖尿病和抗代谢综合征、抗炎、抗肿瘤等有密切关系。
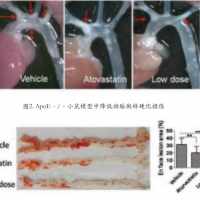
本项目发现物代表性化合物Y9(结构式见图1)对SMS2纯酶的IC50为0.091µM,对SMS1的 IC50为134µM,选择性系数为1400。Y9具有良好的药代性质、较低的毒性和体内外药效,可从降脂、抗炎和抗氧化应激等方面机制发挥抗AS作用。对动脉粥样硬化模型小鼠(apoE–/–小鼠)每天灌胃给药一次,给药7周(剂量12.5mg/Kg),发现与阳性对照药阿托伐他汀(20mg/Kg)一样,能显著地缓解动脉粥样硬化斑块的形成。
另一代表性化合物MY36对SMS2纯酶的IC50为0.100µM,对SMS1的 IC50为56µM,选择性系数为560。MY36Y9具有优良的药代性质。对糖尿病模型小鼠(db/db小鼠)灌胃给药6周(剂量20mg/Kg;50mg/Kg),能从减少炎症因子分泌和抑制炎症通路活化等方面改善糖尿病综合征的作用。
本项目的初步药效、药代动力学性质和作用机制研究实验结果表明,SMS2抑制剂(以Y9和MY36为代表)有着较好的药学特性,毒性小,有较强的体外和体内酶抑制活性,有显著的体内降脂作用,并呈现多重抗动脉粥样硬化作用,还具有抗炎症性糖尿病综合征的作用。这说明了SMS2选择性抑制剂具有进一步研究和开发的价值。2015年调节血脂药物市场达到280亿美元,是仅次于抗肿瘤药物而居于第二位的重要品种。目前列市场销售额前位的调节血脂药物以他汀类为主。预计至2019年销售额较高的仍属瑞舒伐他汀钙和阿托伐他汀。但临床研究证明他汀类药物仅使急性冠脉事件发生率降低30%,并存在着横纹肌溶解等严重不良反应。据2018年7月ThomsonReuters Pharma数据库检索分析,目前处于临床研究的抗AS药物有410个,其中作用机制含降脂、抗氧化、抗炎和抗血栓等。